【お願い】
「こころみ医学の内容」や「病状のご相談」等に関しましては、クリニックへのお電話によるお問合せは承っておりません。
診察をご希望の方は、内科外来の特徴と流れ をお読みください。
骨髄異形成症候群(MDS)の症状・診断・治療
骨髄異形成症候群とは?

骨髄異形成症候群(以下、MDS)とは血液の病気の一つで、骨髄の中にある血液を造る造血幹細胞に異常が起きる病気です。
造血幹細胞に異常を来している細胞を腫瘍細胞とも言いますが、MDSでは腫瘍細胞が増殖する白血病化の側面と、赤血球・白血球・血小板などの正常な血球が造られなくなる無効造血の2つの側面をもっています。
病態によって様々な病型に分類されます。
分類されたそれぞれの病型に異なる病名が付けられているので、「症候群」と言われています。
MDSは造血幹細胞レベルの遺伝子に何かしらの変異を生じることが原因とされていて、この遺伝子変異が原因不明の場合もあれば、化学療法や放射線療法に続発する治療関連MDSの場合もあります。
中高年の男性に発症するケースが多く、40代から次第に増加し、70歳を超えると急激に増加します。
骨髄異形成症候群の症状と予後
MDSは、減少する細胞とその減少の程度によって現れる症状が異なります。
- 赤血球減少:貧血、易疲労感、めまい、動悸、息切れなど
- 白血球減少:易感染状態、発熱など
- 血小板減少:出血傾向、皮膚の点状出血、鼻出血など
一般的な固形癌の様に急激に症状が進行するものではなく、ゆっくり進行するため病気が発症しても症状が現れることなく無症状で経過する場合もあります。
骨髄異形成症候群を疑うきっかけになるのは、鉄欠乏以外が原因の高齢者貧血で、それ以外の血球減少も認められるときになります。
骨髄異形成症候群の予後とは?
MDSは末梢血や骨髄の所見を基に、高リスクと低リスクに分類されます。
無効造血の側面が強い場合は低リスク群とされることが多く、予後は比較的良好です。
白血病化の側面が強い場合は高リスク群とされ、予後不良とされています。
MDSの約1/3は急性骨髄性白血病に移行し、移植が不適応となった高リスク群の予後は半年~1年程度です。
骨髄異形成症候群の診断とリスク予測のための分類
骨髄異形成症候群では、
- 血球(赤血球・白血球・血小板)の減少
を精査していく中で診断されます。
1つの系統だけのこともありますが、2つ以上の系統から疑われます。その他の検査結果として、以下が認められることがあります。
- フェリチン(貯蔵鉄)高値
※鉄欠乏ではない - LDHの上昇
診断にあたっては、骨髄検査が必要になります。
- 末梢血や骨髄内における分化が未熟な幼若血球(芽球)の比率が20%未満
- 造血細胞の異形成が観察される
- 染色体異常
が認められることによって、確定診断となります。
骨髄異形成症候群の予後とは?
骨髄異形成症候群では、タイプによって予後が異なりますし、それによって治療方針が変化します。
このため、病型分類が非常に重要となり、二つの分類があります。
- FAB分類:顕微鏡での見た目の特徴から分類
- WHO分類:FAB分類に遺伝子異常などの新しい知見を取り入れた分類
現在は、WHO分類が使われています。
この違いについては専門的になりすぎてしまうので割愛しますが、WHO分類となって骨髄異形成症候群の定義がしっかりとなされました。
- 異形成は全体の10%以上を占めるとき
- 芽球比率20%以上は急性骨髄性白血病
骨髄異形成症候群のリスク分類
治療方針は、分類されたリスクに応じて決められます。
リスクの分類はIPSSという分類表を用いて行います。
改訂IPSSでは、遺伝子異常に基づく分類がありますが、イメージがつきにくいのでIPSSをご紹介します。

染色体異常と骨髄芽球割合、血球減少の項目の点数を足して合計点数を出すます。点数からリスクがわかります。

骨髄異形成症候群の治療法
おもに3つの治療法があります。
- 支持療法
- 化学療法
- 造血細胞移植
それぞれ、ご説明していきます。
支持療法
根本的な治療ではなく、出現している症状に対して対症的に行う治療法のことです。
- 赤血球輸血:進行した貧血を改善する
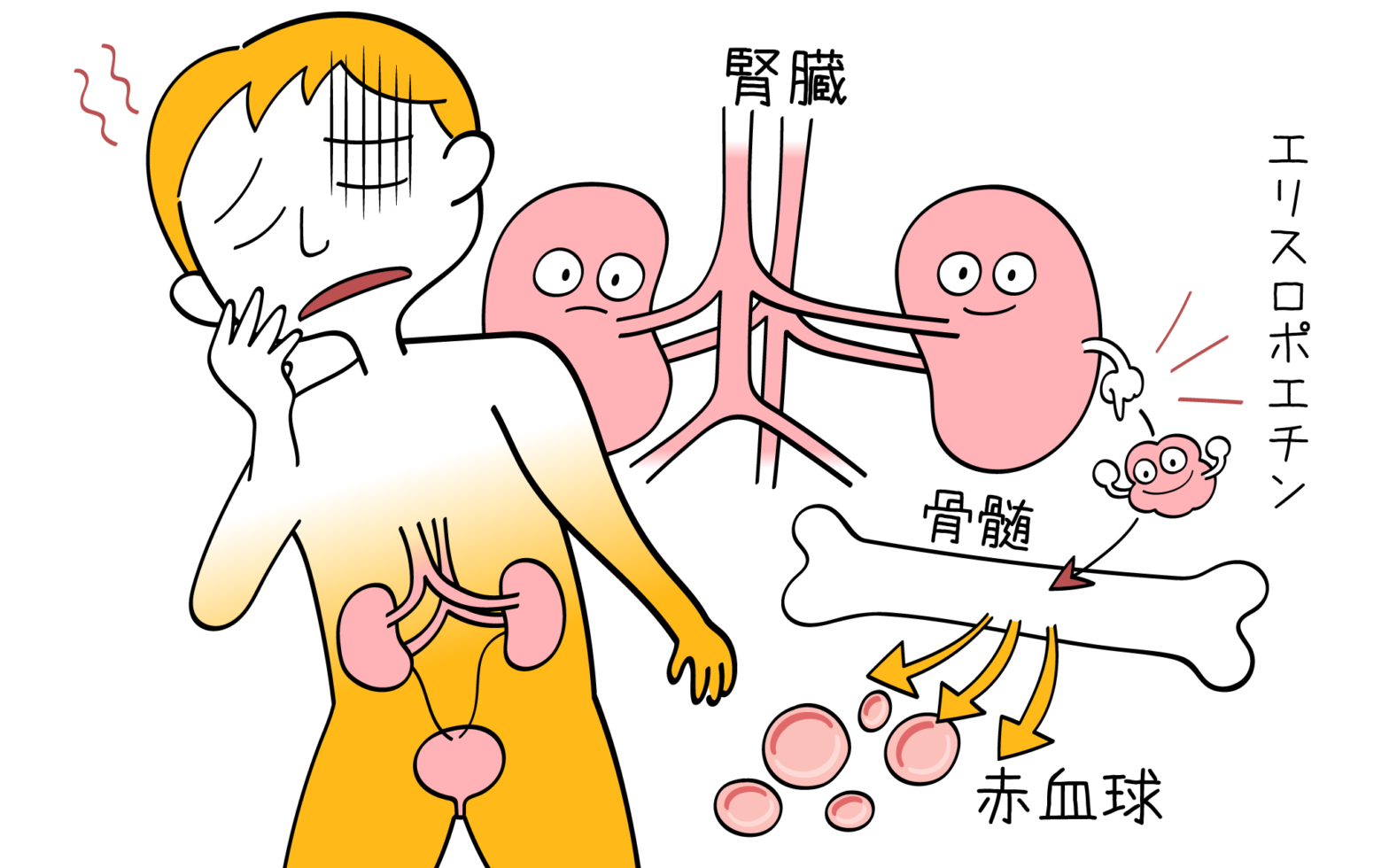
- エリスロポエチン製剤:赤血球を増やす
- 鉄キレート療法:赤血球輸血によって体内で増えた鉄を除去する
- 血小板輸血:出血傾向を改善する
- G-CSF製剤:白血球を増やす
- 抗菌薬:感染の予防目的と治療
化学療法
抗がん剤を用いて腫瘍細胞の増殖を抑制、または死滅させる治療法のことです。
正常な細胞も攻撃することになるので、副作用を伴います。
- 骨髄抑制(血液細胞の減少)
- 悪心嘔吐
- 食欲不振
- 口内炎
- 下痢
- 脱毛
- 倦怠感
造血幹細胞移植
自分が持っている造血幹細胞とドナーの造血幹細胞を総入れ替えする治療法です。
入れ替わった新たな造血幹細胞によって、造血機能の正常化を図ります。
MDSに根治治療はなく、造血幹細胞移植が治癒を期待できる唯一の治療法です。
しかし、造血幹細胞移植は体への負担がかなり大きく、高齢者では適応にならないことも多くあります。
低リスク群の治療方針
無症状、または症状があっても軽い場合は、経過を見ながら必要に応じて支持療法を行います。
症状が目立つ場合や、遺伝子異常があって治療効果が期待できる場合などは、総合的に見て高リスクの治療法も考慮していきます。
高リスク群の治療方針
白血病に進行(転化)してしまう可能性も高いため、積極的に治療を行っていきます。
移植が実施不可能な場合
抗がん剤のアザシチジン(商品名:ビダーザ)が第一選択薬となります。
効果が現れるまでには約半年程度かかりますが、効果がある間は投与を継続します。
通常の抗がん剤に比べ副作用が少ない特徴があります。
アザシチジンの効果がない、または投与できない場合には、全身状態や年齢などを考慮しながら白血病治療に用いる抗がん剤も検討されます。
染色体所見で5番染色体長腕部欠損が判明している場合は、レナリドミド(商品名:レブラミド)という抗がん剤を用いた治療についても考慮されます。
移植が実施可能な場合
年齢やHLA合致ドナーの存在、合併症の有無などを考慮し、可能であれば速やかに造血幹細胞移植を行います。
造血幹細胞移植の流れは、
- 前処置
- 移植
- 移植後の管理
前処置
移植前に多量の化学療法や全身放射線照射などを行い、腫瘍細胞やわずかに残っている正常な血液細胞(主に免疫担当細胞)の根絶を図ります。
この前処置を行うことが、移植後の拒絶反応や疾患の再発を防ぐことにつながります。
移植
②移植
ドナーから提供された新たな造血幹細胞を注入します。
移植後の管理
③移植後の管理
移植後はドナーの細胞が患者(宿主)の細胞を攻撃するGVHDや感染症など、様々な合併症が起こるため管理が重要となります。
【お読みいただいた方へ】
医療法人社団こころみは、東京・神奈川でクリニックを運営しています。
「家族や友達を紹介できる医療」を大切にし、社会課題の解決を意識した事業展開をしています。
上野御徒町こころみクリニックでは、血液患者さんの治療と社会生活の両立を目指し、大学病院と夜間連携診療を行っています。
医療職はもちろんのこと、法人運営スタッフ(総合職)も随時募集しています。
取材や記事転載のご依頼は、最下部にあります問い合わせフォームよりお願いします。
![画像名の[sample]の部分に記事の名前を入れます](https://ueno-okachimachi-cocoromi-cl.jp/wp-content/uploads/2023/01/378123a85308949b14579f3b1dd9a9c4.png)
監修医師紹介
山口 博樹
日本医科大学血液内科 大学院教授/上野御徒町こころみクリニック顧問
日本内科学会/日本血液学会(評議員)/日本造血・免疫細胞療法学会(評議員)
総合内科専門医/総合内科指導医/日本内科学会認定内科医/血液専門医/血液指導医/がん治療認定医/日本造血・免疫細胞療法学会認定医/骨髄移植推進財団ドナー調整医師
![画像名の[sample]の部分に記事の名前を入れます](https://ueno-okachimachi-cocoromi-cl.jp/wp-content/uploads/2025/03/dr_watanabe_s.png)
執筆医師紹介
渡邊 直紀
順天堂大学医学部内科学血液学講座 准教授
日本内科学会/日本血液学会
日本内科学会認定内科医・指導医/日本血液学会認定血液専門医・指導医/日本がん治療認定医機構 がん治療認定医/ICLSインストラクター/日本内科学会総合内科専門医/JMECCインストラクター
カテゴリー:こころみ医学 投稿日:2022年9月29日
関連記事
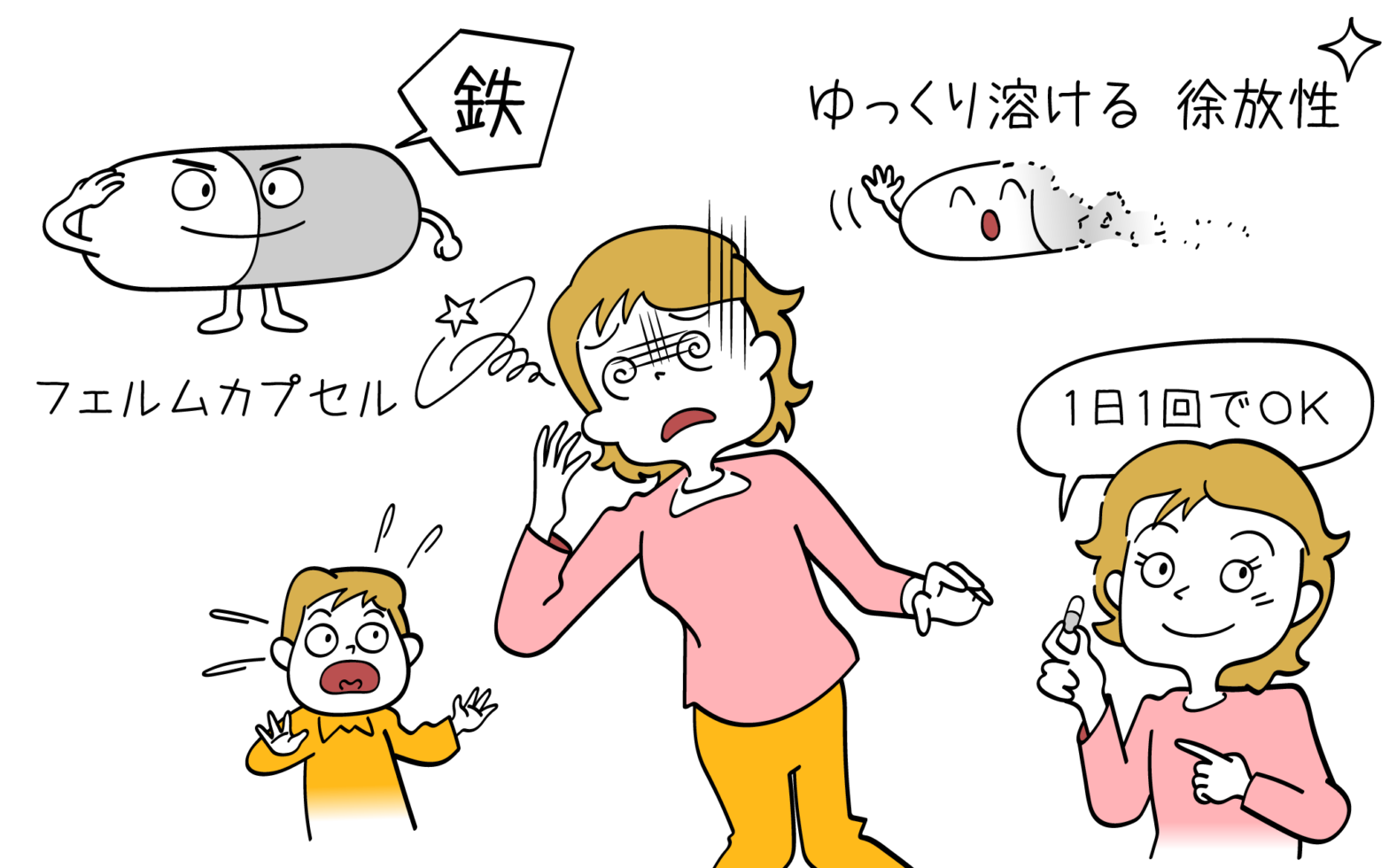
【販売中止】フェルムカプセル(一般名:フマル酸第一鉄カプセル)の効果と副作用
フェルムカプセル(一般名:フマル酸第一鉄カプセル)は、鉄欠乏性貧血に処方されるカプセル剤です。 徐放性の薬剤であり、1日の内服回数を少なくすることで服用の負担を軽減できます。 今回は、フェルムカプセルの効果や副作用につい… 続きを読む 【販売中止】フェルムカプセル(一般名:フマル酸第一鉄カプセル)の効果と副作用
投稿日:
人気記事

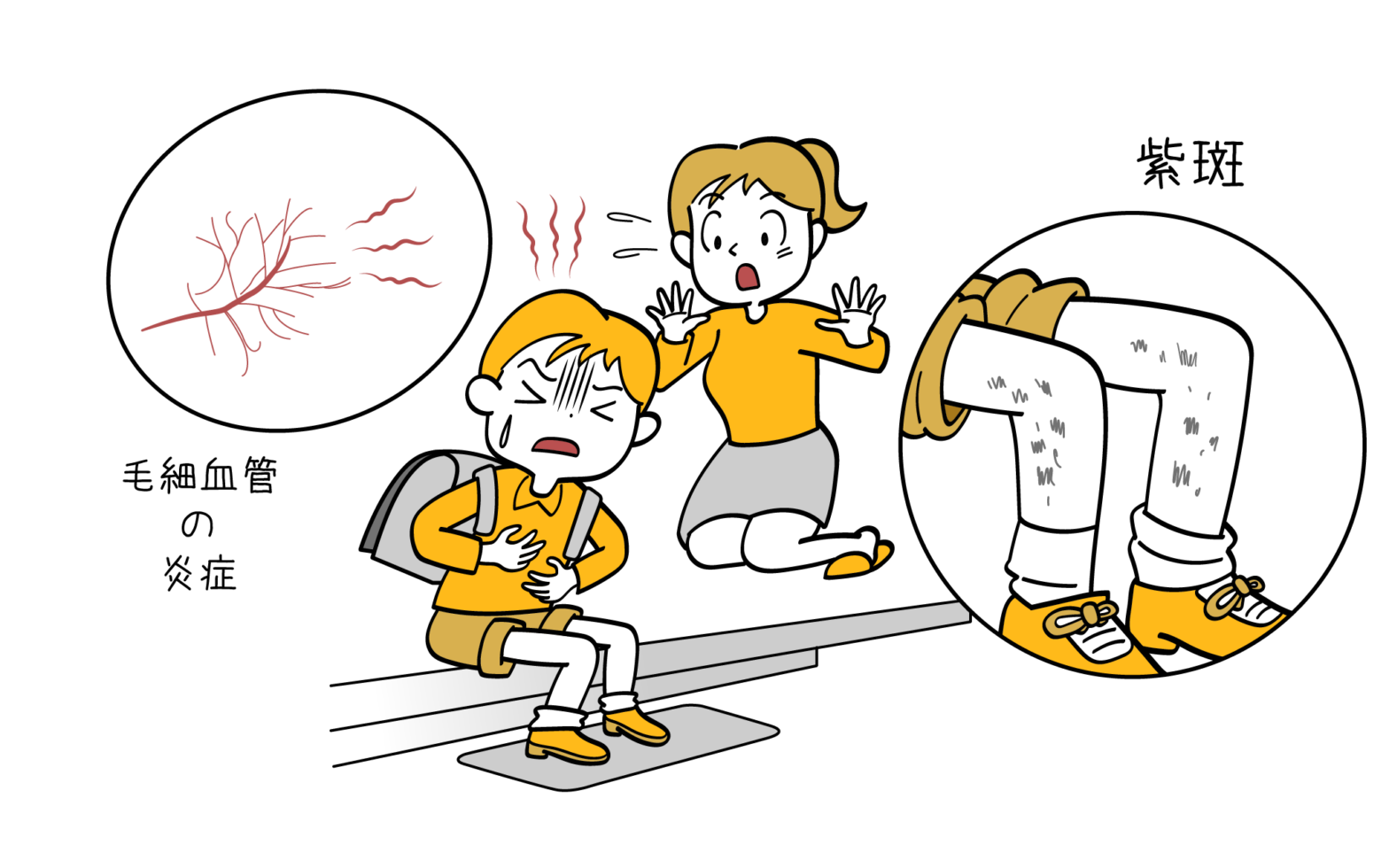
紫斑病の症状・診断・治療
紫斑病とは? 紫斑病とは、止血に重要な働きをしている血小板が減少してしまうことなどで、血が止まりにくくなっているときに起こります。 その原因は様々で、血小板の機能に異常がある場合、凝固因子といわれる止血に必要なタンパクが… 続きを読む 紫斑病の症状・診断・治療
投稿日: